自閉症リスク因子が脳発生に与える影響を一網打尽に!


 興味深いのが赤丸で囲ったAnk2, Chd8, Gatad2bの3遺伝子である。
興味深いのが赤丸で囲ったAnk2, Chd8, Gatad2bの3遺伝子である。
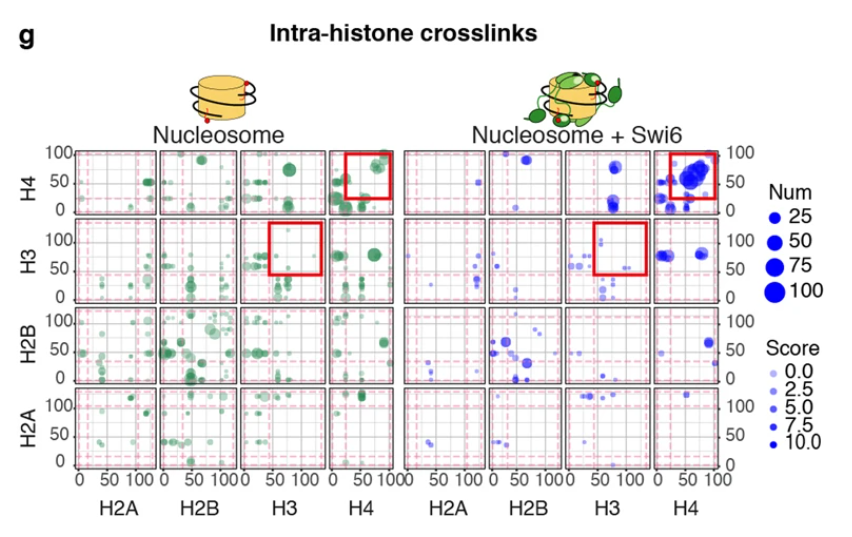
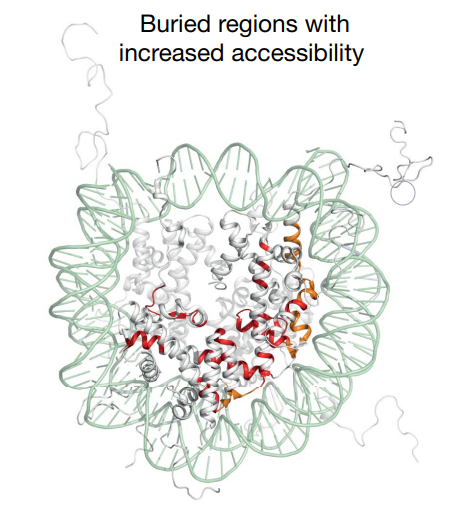
相分離を駆動する"ヌクレオソームコア"の構造変化

真のオス化遺伝子の発見!?
今回珍しく日本人の方の論文を紹介させていただきます。関係者の方(に限らず)間違いなどございましたらご指摘いただけると幸いです。
----
性別をきちんと決定することは種の生存及び進化に非常に重要である。
これまで哺乳類のオス化を決定する遺伝子としてY染色体上のSryという遺伝子が同定されてきた。
Sryはその発見以来、単一のエクソンからなる遺伝子だと考えられてきた。
今回、Sryにこれまで未知であった第2エクソンが存在し、オス化に重要であることを示した論文を紹介する。

-----
まず、筆者らはRNAシーケンスを行うことで、Sry遺伝子座近傍で発現しているRNAを解析した。
このとき、通常であれば解析の段階でゴミとして切り捨てる「複数のゲノム領域に貼り付きうるリード」を捨てずに解析することで、これまで報告されてこなかったSry近傍の転写物を発見した。
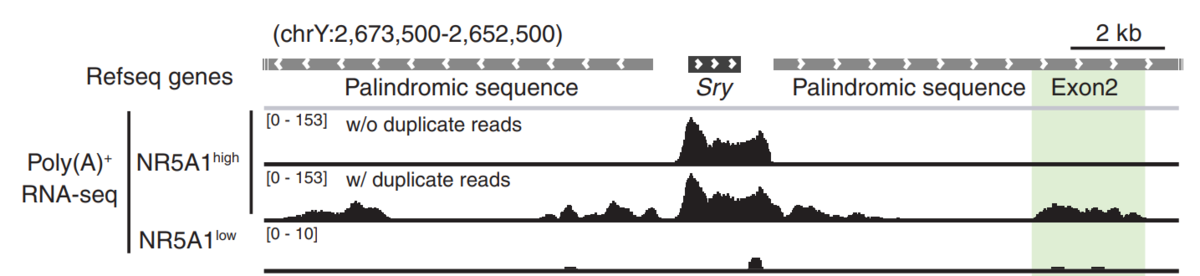
(Sry遺伝子座は回文配列に挟まれ、平たく言うと面倒くさいゲノム領域に存在することから、マルチマップを許さないと見えてこなかったのだろう。いやー、マルチマップを許してみようと思う発想がすごい。)
筆者らはさらに転写開始点を特定可能なRNAシーケンス(CAGE-seq)や、タグをノックインしたマウスの作成を行うことで、このSry近傍の転写物はこれまでないとされてきたSryの第2エクソンであることを明らかにする。
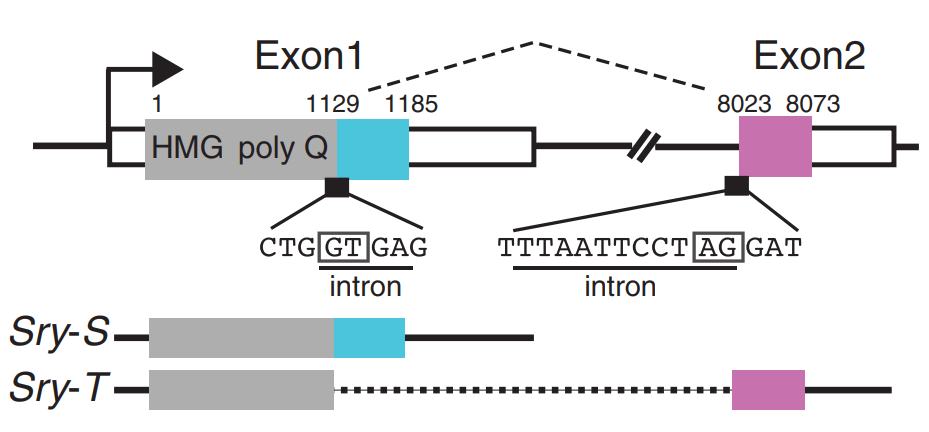
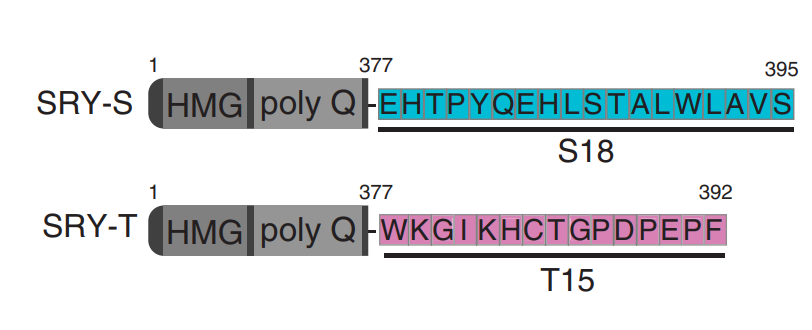
筆者らはこれまでの単一エクソンからSryをSry-S(Single)、新しく同定した第2エクソンを含むSryをSry-T(Two)を名付けている。
Sry-TはSry-SのC端18アミノ酸が欠損し、新しく15アミノ酸を獲得したアミノ酸配列になっている。(以下の図を参照)
----
では、この第2エクソンを含むSry-Tは性決定に重要なのだろうか?
筆者らはSryの第2エクソンを削るようなマウスを作成し、解析を行った。
すると驚くべきことに、Sryの第2エクソンを削ったマウスでは染色体がXYであってもメスのようになることが分かった。
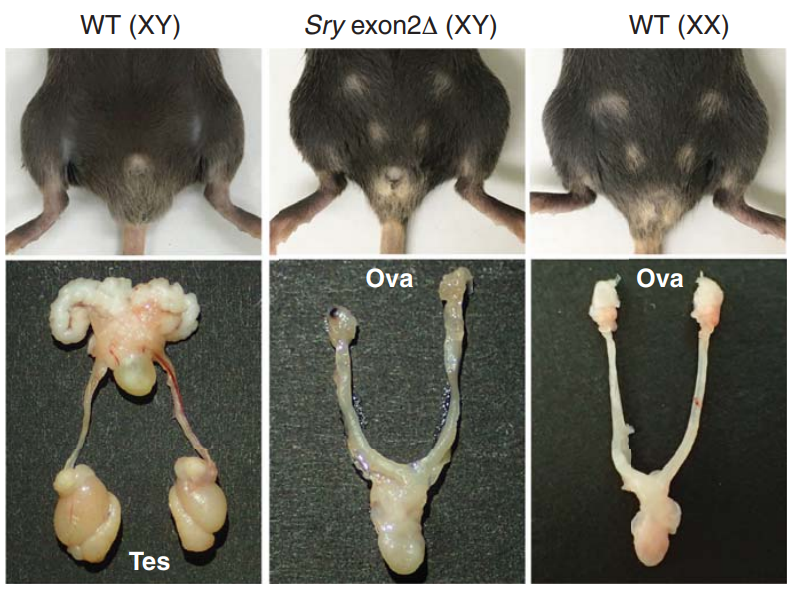
このことから、Sry-Tはオス化に必須の働きをすることが分かった。
---
さらに筆者らはSry-Tを発現するだけでオス化を誘導できるのか検証するため、XX染色体をもつマウスで生殖細胞特異的にSry-SおよびSry-Tを強制発現させ、解析を行った。
その結果、Sry-Sをヘテロで発現するマウスはメスのままであるのに対し、Sry-Tを発現するマウスはオス化することが分かった。
すなわち、Sry-Tの発現はマウスのオス化に十分であることが分かった。
-----
では、Sry-TはSry-Sと何が違うのだろうか?
興味深いことにSry-Sだけが持っているC末端のアミノ酸配列は、タンパク質分解メカニズムによって分解を受けやすい配列であることを見出した。
実際、蛍光タンパク質にSry-SのC末端の配列を付加すると安定性が(Sry-Tの末端配列を付加した場合に比べて)減少することを示している。
このことから、Sry-Tはタンパク質として安定であるためにオス化を誘導できる可能性が考えられる。
この可能性を検証するため、筆者らはSryの第2エクソンを削ったうえで、Sry-Sのタンパク質分解誘導配列に変異を加えたマウスを作成した。
Sryの第2エクソンを削ると染色体がXYでもメスになるが、さらにSry-Sのタンパク質分解誘導配列に変異を加えるとオス化することが分かった。
すなわち、Sry-TはSry-Sに比べタンパク質が安定である可能性が高く、その特性こそがオス化に重要である可能性が示唆された。
----
結果は大体以上で、今回筆者らによりこれまで見つかっていなかったSryの第2エクソンが見つかり、この第2エクソンを保持するタイプのSry-Tこそがオス化に重要であることがわかった。
どうやらこの第2エクソンはトランスポゾン由来の配列らしく、一度挿入が起こったのち、進化に有利な配列として残ったのだろう。
----
管理人コメント
・本当にとってもすごい!!RNA-seqのマッピングで重複を許して第2エクソンを発見し、マウスの劇的な表現型の発見にとどまらず、そのメカニズムにまで迫っていて震える。
・マッピングで重複を許したら見えてくるタンパク質とかまだまだあるのだろうか。本当にゴミだと思って捨てていたリードからすごいものが見つかったりして、、
今回紹介した論文
The mouse Sry locus harbors a cryptic exon that is essential for male sex determination
タンパク質ノックダウンで見えてきた新しい転写制御機構

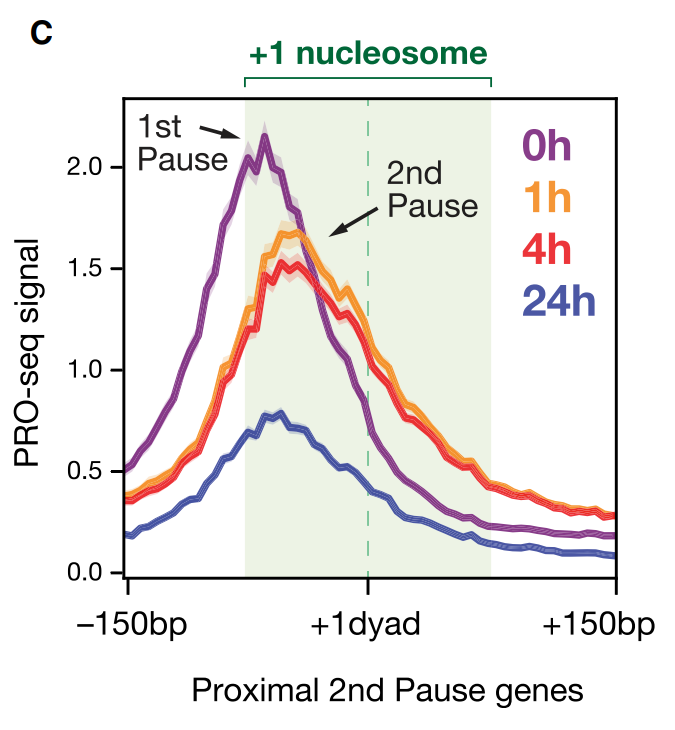
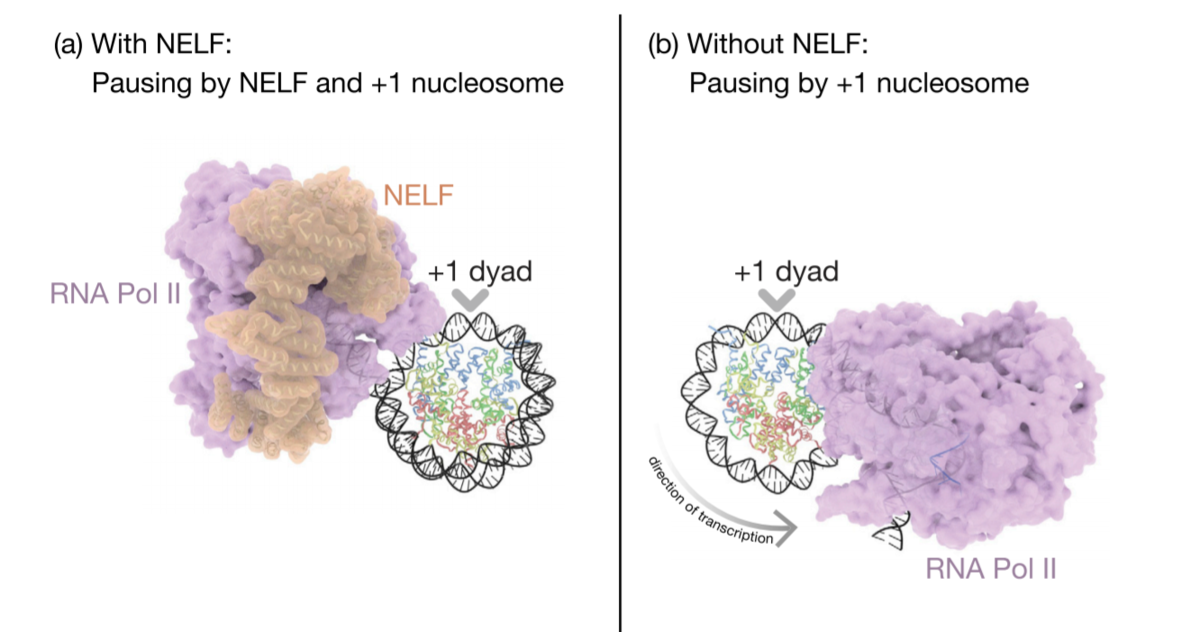
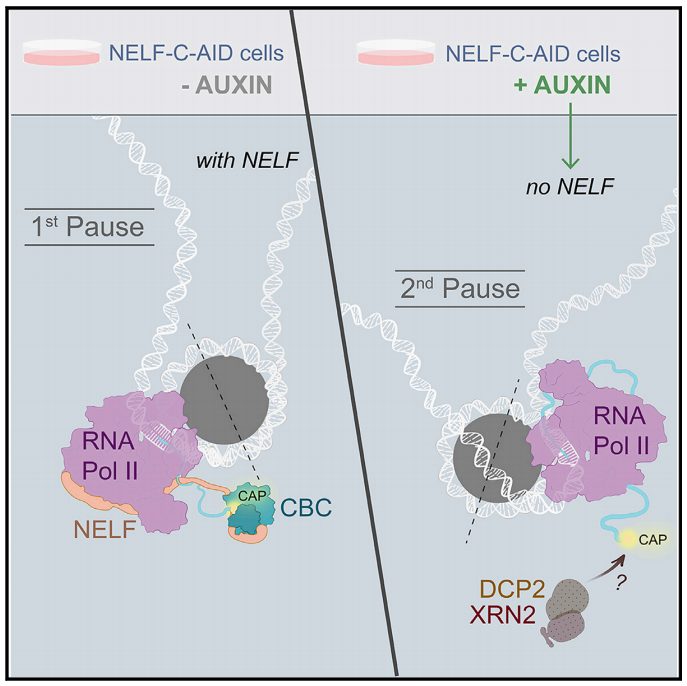
-----
2020年ノーベル医学生理学賞;C型肝炎ウイルスの発見



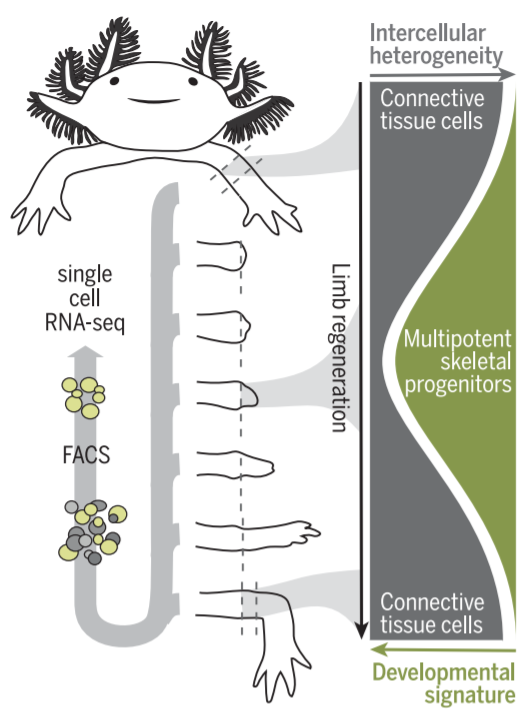
再生に伴う遺伝子発現のダイナミックな変動
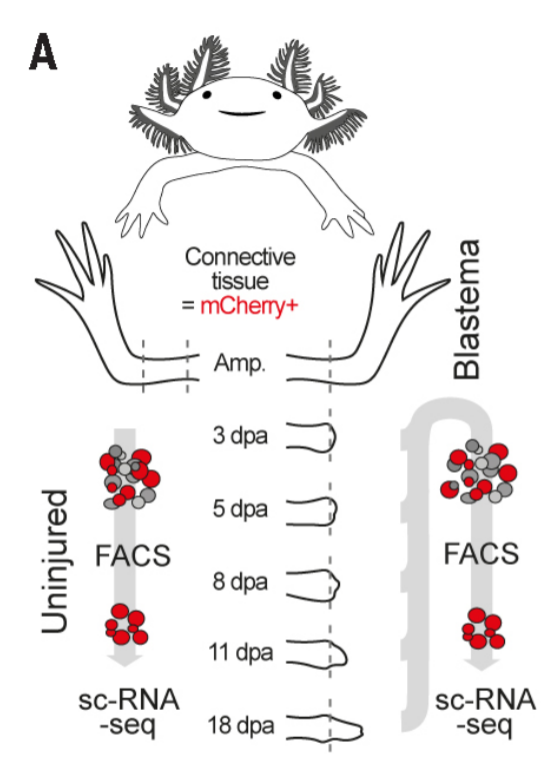
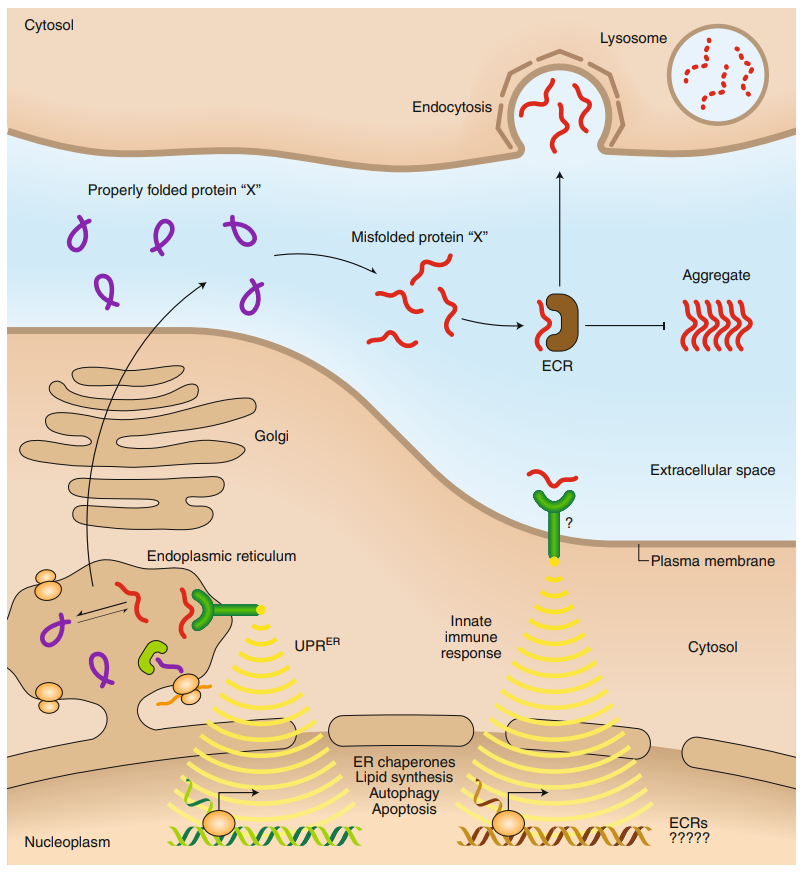
細胞外タンパク質の品質管理