ヒストン修飾と相互作用する新規タンパク質の網羅的同定
正確な細胞運命の制御には、正確な遺伝子発現の制御が重要である。
厳密な遺伝子発現の制御のために、DNAを巻き付けるヒストンのメチル化やアセチル化といった化学修飾が大きな役割を果たすことが知られている。
これまでにヒストンの化学修飾(メチル化/アセチル化など)を触媒する酵素や、認識するタンパク質がいくつも同定されてきた。
しかしながら、細胞内で特定のヒストンの化学修飾と相互作用するタンパク質を網羅的に探索する方法は十分には整備されていない。
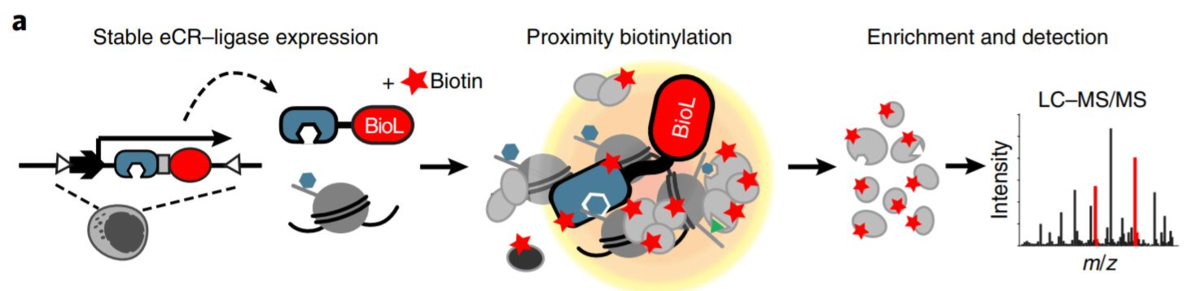
そこで今回人工的なヒストン修飾認識ペプチドとビオチン化酵素を組み合わせ、ヒストン修飾近接タンパク質を網羅的に解析した論文を紹介する。(短め)

-----
まず筆者らは特定のヒストン修飾に目印をつけるため、人工的なヒストン修飾認識ペプチド(engineered chromatin readers, eCRs)を以下のように設計した。
H3K27me3...CBX7のクロモドメイン
H3K9me3...CBX1のクロモドメイン
H3K4me3...TAF3のPhdドメイン
DNAメチル化...MBD1とMeCP2のMBDドメイン
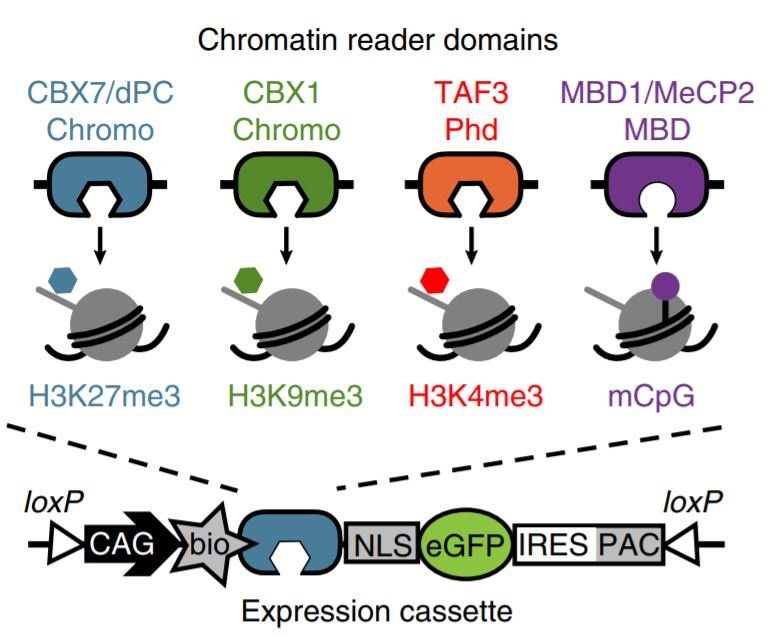
(実際これらが標的したヒストン修飾と共局在することを丁寧にみている)
この結果、H3K9me3に近接するタンパク質として、既知の因子以外にZNF転写因子群を同定している。
実際この一つであるZNF280Dにタグをつけてゲノム上での局在みるとH3K9me3と共局在する。
もちろんこれ以外にも、H3K27me3, H3K4me3, DNAメチル化, bivalentに近接する新規因子をたくさん同定している。かなりすごい。
面白いのはH3K27me3にH3K9メチル化酵素が近接しているという結果で、ヒストン修飾間の相互作用がありそうというのを示唆している。
(他にもいろいろ結果だしている細かいので省略。興味ある方は元論文を参照ください。)
---
そういわけで、ChromIDで細胞内で特定のヒストンの化学修飾と相互作用するタンパク質を網羅的にみれるらしい。実際未知の近接タンパク質もとれているのですごい。
vivoでやるならプラスミドで過剰発現するかChromID用の配列がノックインされたマウスを作らないといけないのでちょっと面倒かも。
ところで、そもそもヒストン修飾でChIPしてMSするようなことはあんまりされてこなかったのか?と思っていたらRichard A. Youngのグループが2015年に出していた(PNAS, 2015)。
今回の論文ではせっかくならChIP-MSとChromIDの比較も出してほしかった。まあいいんだけど。
-----
以下、特定の配列やヒストン修飾に結合するタンパク質を網羅的に解析する手法のまとめ。(さくっと見つけられたもののみ。。)
PICh法...proteomics of isolated chromatin segments (Robert E.Kingston group, Cell, 2009)
CAPTURE法...CRISPR affinity purification in situ of regulatory elements (Jian Xu group, Cell, 2017)
PICh法に似ているがCas9を使用したシステム。1コピーの遺伝子座にも使える。論文ではグロブリンのスーパーエンハンサー配列について解析。
CasID法 (Heinrich Leonhardt group, Nucleus, 2016)
アイデアはCAPTURE法と同じでCAPTUREより1年早い。。。おそらく1コピーの遺伝子座に応用できていなかったのでCellにはならなかったのだろうか。
SNAP法...SILAC nucleosome affinity purifications (Tony Kouzarides group, Cell, 2010)
ヒストンを化学修飾した再構成ヌクレオソームを細胞内に入れてプルダウンする手法。
シングルセルRNAseqなどの-seqの爆発的な流行の裏で、細胞運命を制御する実際的な実行因子であるタンパク質の解析はむしろ進みが遅くなっている気もしなくはない。
-----
今回紹介した論文 (画像はすべて論文より引用)
ChromID identifies the protein interactome at chromatin marks, Nat. Biotech., 2020 (リンク)