ゲノム中の塩基配列の偏りの意義?
生物のゲノムはATGCの4つの塩基の組み合わせからなる。
このA, T, G, Cはゲノム中に均等に存在するわけではなく、ある一定の偏りを持って並んでいる。
では、この塩基の配列の分布の偏りは何か役割を持つのだろうか?
これまでCG配列に結合する因子とその機能がいくつか報告されてきた。
このためCG配列が多いことには何らかの意味があることが示唆されてきたが、AT配列については比較的その意義は調べられてこなかった。
今回、ゲノム中のATが濃縮する配列を読み取り、細胞運命を制御する因子を同定した論文を紹介する。
筆者らはまず、ATが多いDNAに結合する因子を網羅的に探索した。
この結果、これまでATに結合することが知られていた因子を含め、複数の因子がヒットした。
筆者らはこの中からSall4という因子に着目した。
SALL4は神経/四肢などの発生に重要な因子で、ヒトではオキヒロ症候群という疾患と関連していることが知られている。
----
ではSall4がATに多い遺伝子座に結合することは遺伝子発現にどのような影響を与えるのだろうか?
この結果興味深いことに、Sall4の機能欠損ではATが多い遺伝子の発現が上昇し、Sall4の過剰発現ではATが多い遺伝子の発現が減少することが分かった。
このことからSall4はATが多い遺伝子の発現を抑制している可能性が示唆された。
----
さらに筆者らはSall4がATの多い遺伝子に結合する生物学的意義を探索した。
このために、筆者らはSall4のDNA結合部位に点変異を導入したマウスを作成した。
Sall4のノックアウトマウスは胎生致死になることが知られていたが、なんと今回作成された点変異マウスも胎生致死になることが明らかになった。
このことから、Sall4がATの多いゲノム領域に結合することは正常な初期発生に重要である可能性が示唆された。
----
結果は以上のような感じで、今回の結果から
・Sall4がATに偏ったゲノム領域に結合し、遺伝子発現を抑制することで正常な発生を可能にする
というモデルを提唱している。
彼らのメッセージとしては
・それぞれの遺伝子座に固有のゲノム配列から遺伝子を個々に制御するより、塩基の分布の偏りを読み取ってまとめて遺伝子発現を制御するほうが合理的だよね
ということらしい。まあそうかもしれない。
以下グラフィカル
----
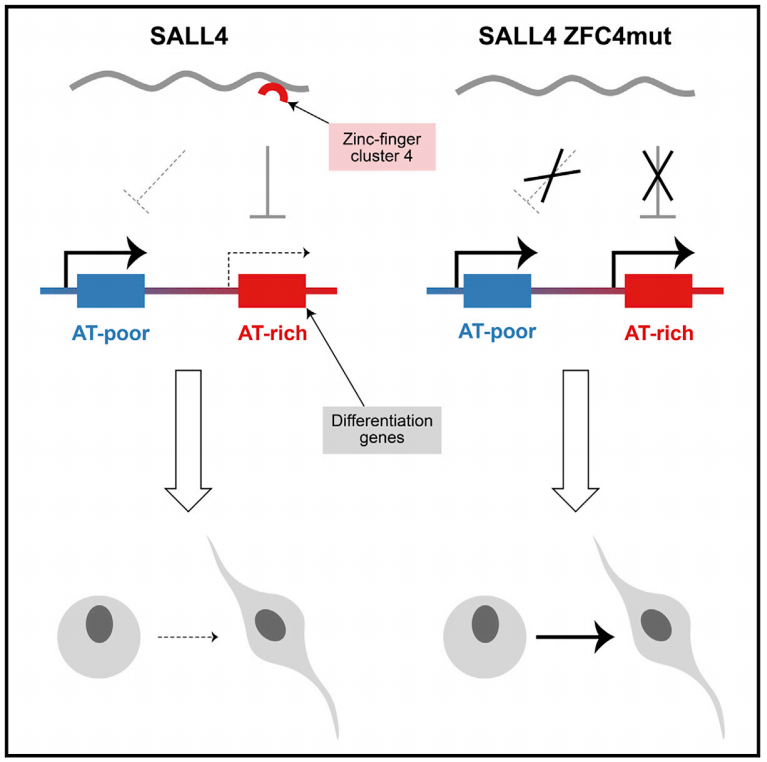
----
コメント
・Sall4の(AT結合ドメインの)機能解析を"ゲノム中のATの偏りの意義"と概念的に発展させているのは勉強になった。やはり一般的なメッセージにするのは大事だな。(結果から十分サポートされているかはやや疑問)
イマイチわからなかったこと(解決した方は教えてください!!)
・Sall4結合領域と発現制御する遺伝子の遺伝子座の関係が不明瞭。載っているデータでSall4結合領域→AT rich、Sall4変異で発現上昇→AT richはいいが、Sall4変異で発現変動⇔Sall4結合は不明。いかにもSall4が直接AT rich geneを抑制しているように書いているが、間接的な可能性もあるのでは?
・ATの比を反映して遺伝子発現制御と主張しているが、Sall4がATの比だけでゲノムにターゲティングしているとは思えない。ATはクロマチン閉じている印象だが、彼らはSall4はオープンクロマチンに濃縮することも示しているしSall4の結合には配列以外の因子も関係ありそう。"ATの比を反映して"というにはデータ薄い?
SALL4 controls cell fate in response to DNA base composition, Mol. Cell, 2020