ニューロンは特別ではない?_1





肥満が摂食のブレーキを外す!?

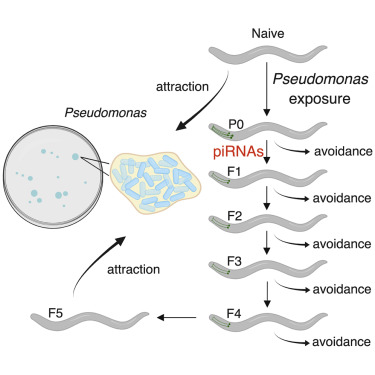
記憶が遺伝する!?
「現在地」と「目的地」の情報は脳内でどのように処理されているか(筆頭著者による論文紹介)
筆頭著者による論文紹介第2弾、東大薬の青木さんにご寄稿いただきました!
メディア出演などでもおなじみの池谷裕二研究室に所属されています。
とても丁寧にご解説頂きましたので是非最後までご覧ください!
-----
初めまして。東大薬の青木と申します。私は現在、海馬に存在する場所細胞と呼ばれる神経細胞について研究を行っています。
このサイトでこれまで紹介されている分野からは少し離れる話題になってしまいますので、簡単に研究の背景を含めつつ、論文紹介をさせていただこうと思います。このような機会は初めてですので至らない点も多いかと思いますが、よろしくお願いいたします。
2014年のノーベル生理学・医学賞は海馬の場所細胞(place cell)を発見したJohn O'Keefと、嗅内皮質の格子細胞(grid cell)を発見したMoserらに授与されました。
O’Keefeらが場所細胞について初めて報告したのは1971年のことです。彼らは、ラットの海馬に記録電極を埋め込み、自由行動下にて、海馬の興奮性錐体細胞の発火活動を記録する実験を行いました。その結果、海馬の興奮性神経細胞の一部が、ラットが特定の位置(place field)にいる時にのみ発火頻度を上昇させることが発見され、場所細胞(place cell)と命名されました(図1)(場所細胞という名前の細胞種があるわけではないことに注意してください。
ある環境内において、動物の場所に依存して発火を示す興奮性神経細胞が場所細胞と呼ばれます。異なる環境に動物を提示するとさっきまで場所細胞として活動していた細胞が場所依存的な発火を示さなくなることや、その逆に新たに場所細胞として活動し始める細胞も存在することが知られています(リマッピング(Leutgeb et al., 2005))。場所細胞というよりは“場所依存的な活動を示す興奮性神経細胞”の方が正しい気もしますが場所細胞と呼ばれています)。

当時は海馬の破壊実験などによって、海馬が空間学習や空間認知に重要な役割を果たすことは示唆されていました。その中で、海馬場所細胞の発見は、脳内の空間表象を担う細胞単位を発見したという点で非常にインパクトのあるものでした。O’Keefeらは1978年には「認知地図としての海馬」という題名の本を出版し、場所細胞が、動物の空間認知地図(cognitive map)の要素であるとの理論を提唱しました。
現在でも、この認知地図の理論は支持され続けています(上で述べたリマッピングは、異なる環境に動物を提示することで、異なる認知地図がリクルートされているためだと考えられます。ある細胞集団によってある環境に関する地図が作られているイメージです。)。動物の行動と神経活動の相関が非常にきれいに見られるため、脳の情報処理機構を捉えるための研究が場所細胞を用いて行われています。
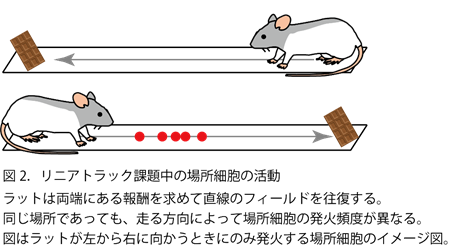
さて、このように脳内の空間表象を担う基盤として考えられてきた場所細胞ですが、実は純粋に動物の場所の情報のみに依存して発火を示すわけではないことが知られています。最も単純な研究例としては、一本道の上を行動するリニアトラック課題があります。ここではラットが道の両端に交互に置かれた報酬を得るために繰り返し行き来します。こうした条件で海馬の神経細胞の発火パターンを記録すると、当然、場所選択的な活動が記録されますが、同じ場所を通過しているときでも、走る方向によって各細胞の発火頻度が大きく異なることが報告されています(Aghajan et al., 2015)(図2)。では、このような場所選択的な活動はどのようにして生じているのでしょうか。
単純に考えられることとしては、海馬場所細胞が場所(現在地)の情報だけでなく、これから向かう場所がどこかという目的地の情報にも依存して発火している可能性があります。また、場所とラットの頭部方向の両方に依存して発火しているのかもしれません。(実際に海馬の上流である嗅内皮質には、動物の頭部方向に依存して発火を示す頭方向細胞(Head direction cell)が存在することが知られています。) しかし、一本道の上を歩くリニアトラック課題では、ラットの行動(頭部方向)と目的地が1対1で結び付けられてしまっているため、これら2つの条件を区別することが出来ません。
これを解決する単純な方法は、ある1つの目的地に対して複数の方向から動物を走らせてみることです。そうすればこの場所細胞が、目的地に依存して発火する(図3上)のか、それとも頭部方向に依存して発火する(図3下)のかを区別することが出来そうです。

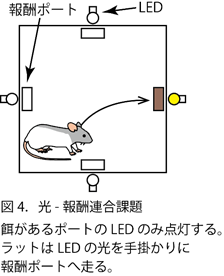
実際にそのような行動を動物に行わせるために、新たに行動試験系を設計しました。それが図4のようなものです。1メートル四方のフィールド内に報酬ポートが4箇所存在しており、それぞれのポートから報酬(餌)が提示されると、ポートの上部に設置した白色LED光が点灯します(光-報酬連合課題: Cued task)。(Arduinoなどを用いて報酬ポートなども全て自作しました)。
2週間ほどこの行動試験を行わせると、ラットは光と報酬の関係を学習し、LEDの光を目的位置として、各報酬ポートへ一直線に走る目的地指向型の行動(Goal-directed behavior)を示すようなりました。この行動試験中に海馬の神経細胞の発火パターンを記録すると図5のようになっており、頭部方向ではなく、目的地に依存して発火する場所細胞が存在することを確認しました。これは海馬場所細胞が自分の現在地の情報に加えて、自分がどこに向かっているのかという目的地の情報にも依存して発火することを示しています。

次に、この目的地指向型の発火を示した場所細胞が、目的地の存在しない場合にどのような発火を示すかについて調べました。報酬ポートやLEDを取り除いたフィールドにラットを再提示し、海馬の神経細胞の発火を記録してみました(擬似探索課題)。この条件では、フィールド上のランダムな場所で報酬を提示したため、ラットはもはや報酬ポートに対する目的地指向型の行動を示さず、フィールドをうろうろ探索するような行動を示すと想定していました。基本的には想定通りにラットは探索行動を示しました。しかし、時々、前回の課題の条件を思い出したかのように、かつて報酬ポートが置いてあった場所に向かって真っ直ぐ走るような行動を示しました(図6中央)。

この行動は非常に面白いものと感じました。なぜなら、先ほどまでの目的地の存在するフィールドで記録した条件も含めると、ラットの行動を3種類に分類できるためです。つまり、①目的地が存在し、ラットも目的地に向かおうとしている、②目的地は存在しないが、ラットは目的地に向かおうとしている、③目的地が存在せず、ラットにも特に目的地はない の3つです(図7)。これまで行われてきた場所細胞の研究では①と③の比較を行っているものは多いですが、②のような条件で記録が行われたものはほとんどありません。動物の動機、モチベーションと神経活動の相関についての記述を目指し、②の行動について詳しく調べることにしました。

②のような行動(pseudo-Goal-directed behavior)は、人の目で見ればある程度判定することはできますが、特定の条件(速度が~cm/sec以上で、頭の方向が報酬ポートが置いてあった方向を向いてて、~sec以上その方向に走り続けてて…みたいな)を用いて分類しようとするとかなり難しかったです。初投稿時には上記のような条件を設定して無理やり分類していましたが、Reviewerや先輩からの助言により、tsneと呼ばれる次元削減アルゴリズムを用いて分類を行いました。これにより、各パラメータをかなり適切に決定することが可能になり、納得のいく結果を得ることが出来ました。さて、②の行動時の神経活動を調べてみると、目的地が存在していないにも関わらず、①の行動時に見られていた、目的地指向型の発火と非常に類似した発火が生じていました(図8)。つまり、目的地指向型の発火は目的地の有無にかかわらず、ラットの動機、モチベーションによって生じることを示唆する結果を得ることが出来ました。
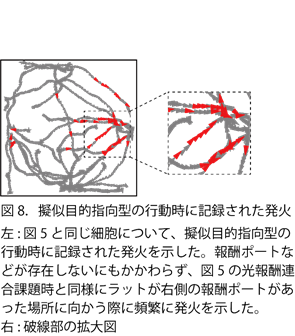
さらに、探索行動時の場所細胞の発火率と、目的地指向型の発火率を比較してみると、目的地指向型の発火率の方が高いことがわかりました。つまり、探索行動時には、場所の情報を処理するような入力を受け取っていた場所細胞が、目的地に向かおうとしている際には、場所の情報を処理するような入力と目的地に関する情報の入力を受け取り、発火率を増加させていると考えられます。
では、この目的地に関する情報はどのようにして海馬に入力されているのでしょうか。ラットが走っている際、海馬ではシータ波と呼ばれる特徴的な脳波が生じることが知られています。このシータ波は内側中隔と呼ばれる脳領域からの入力により生じることが明らかにされています。そこで、内側中隔にムシモールという試薬を投与し、内側中隔の活動を抑制した状態で、行動試験を行わせ、海馬の神経活動を記録してみました。すると、目的指向型の発火が低下するという結果が得られました。この結果は、内側中隔の活動が、海馬へ目的地に関する情報が入力されるために重要であることを示唆しています。
以上の結果、
- 海馬で目的地指向型の発火が生じること(海馬場所細胞は、動物が目的地に向かう際に発火率を上昇させること)(論文Fig. 2, 3, 5)
- 動物の内的なモチベーションによって発火率の上昇が生じること(論文Fig. 4, 5)
- 内側中隔の抑制によって目的地に向かう際の発火率の上昇が抑制されること(論文Fig. 6)
をまとめて論文として投稿いたしました。
なるべく簡潔に説明しようと努力したつもりですが予想以上に長くなってしまいました。おそらくこの記事は分野外の方から読まれる機会が多いと思いますので、少しでも場所細胞に関する研究の理解の助けとなれれば幸いです。
近年、場所細胞の研究に強化学習の目線を取り入れることで、動物の行動戦略の理解を目指しているような研究も行われています(Stachenfeld et al., 2017)。今後の研究によって、動物の行動や学習、記憶の基盤となるメカニズムの解明が進むことを期待しています。
Reference
Aoki Y, Igata H, Ikegaya Y, Sasaki T. (2019). The Integration of Goal-Directed Signals onto Spatial Maps of Hippocampal Place Cells. Cell Rep. 5, 1516-1527.
Leutgeb S, Leutgeb JK, Barnes CA, Moser EI, McNaughton BL, Moser MB. (2005). Independent codes for spatial and episodic memory in hippocampal neuronal ensembles. Science. 309, 619-23.
Aghajan ZM, Acharya L, Moore JJ, Cushman JD, Vuong C, Mehta MR. (2015). Impaired spatial selectivity and intact phase precession in two-dimensional virtual reality. Nat. Neurosci. 1, 121-8.
Stachenfeld KL, Botvinick MM, Gershman SJ. (2017). The hippocampus as a predictive map. Nat. Neurosci. 11, 1643-1653.
------
バイオステーションでは、筆頭著者の方による論文紹介を募集しています。どのような分量でも構いませんので、ぜひご寄稿いただけると幸いです。
詳細につきましては、以下のリンクもご覧ください
筆頭著者による論文紹介第一弾はこちら
ペルオキシソームの新しい機能を発見! (筆頭著者による論文紹介)
今回、筆頭著者による論文紹介、ということで、東大薬の田中秀明さんにご寄稿いただきました!
比較的マイナーなオルガネラ、ペルオキシソームの新しい機能を発見したという報告です。とても丁寧に書いていただきました!ぜひ最後までご覧ください!
-----
ペルオキシソームの新しい機能を発見!-ミトコンドリアの動態・細胞死経路の制御-
皆様、ペルオキシソームというオルガネラをご存じでしょうか?
ペルオキシソームはほぼすべての細胞がもつ脂質一重膜で覆われたオルガネラであり、主に脂肪酸の酸化や活性酸素の除去といった細胞の代謝機能を担うことが知られています。
細胞内において、ペルオキシン遺伝子群によって形成されています。ペルオキシン遺伝子群が欠損することで、ペルオキシソームの機能不全が引き起こされます。ヒトにおいて、ペルオキシン遺伝子の欠損は、ツェルベーガー症候群をはじめとする非常に重篤な疾患の原因となります。ツェルベーガー症候群の患者は筋緊張低下、顔面形成異常、神経遅滞など多臓器にわたる影響が表れ、重篤な場合では出生後一年以内に死亡してしまいます。
このことから、ペルオキシソームが生体内で重要な役割を果たしていることは明らかです。しかしながら、ペルオキシソームの機能解析はあまり進んでいません。恐らく読者の方も、「教科書で見た気がするけど、あまり覚えてないな」くらいの認識ではないでしょうか?
私は、この重要だけれど謎の多いオルガネラ、ペルオキシソームに注目し、その機能解析を行うことにしました。はじめは何に注目すればいいかわからず、暗中模索の時期もありましたが、最終的にミトコンドリアとの新たな相互作用を見出し、論文としてまとめることができました。ここでは、代表的な結果を紹介しつつ、どのように自分の研究が進んでいったかをまとめてみたいと思います。参考にしていただければ幸いです。
---
ペルオキシソームの機能を探索すべく、まずペルオキシソーム形成に必須の遺伝子Pex3をCRISPR-Cas9システムでKOし、ペルオキシソーム欠損細胞を樹立しました。免疫細胞染色を行うと、実際この細胞ではペルオキシソームが完全に消失していることが観察されました。
ここで、とりあえずほかにもいろいろなオルガネラを染色してみよう、ということになり、小胞体、ゴルジ体、ミトコンドリアなど様々なオルガネラを観察してみました。色々と面白いことが分かったのですが、一番大きな表現型が「Pex3のノックアウトによってミトコンドリアが顕著に断片化している」というものでした。この現象は面白い!と思い、ペルオキシソームによるミトコンドリア動態への影響についてさらに調べることにしました。
ペルオキシソームが本当にミトコンドリアの動態制御にかかわるのか?ということをさらに調べるため、ペルオキシソームの十分性について検討することにしました。ここで用いたのが、4-PBA(4-フェニル酪酸)です。これは、PPARシグナルとPex11の経路を介してペルオキシソームを増加させる薬剤です。これを細胞に添加すると、実際にペルオキシソームが増加することが観察されました。この時、ミトコンドリアの形態はどうなっているかというと、驚くべきことに4-PBAによりミトコンドリアが顕著に伸長する像が観察されました。この4-PBAによるミトコンドリアの伸長が本当にペルオキシソームを介しているかを調べるため、同じ実験をペルオキシソーム欠損細胞で行うと、通常細胞で見られたミトコンドリアの伸長は観察されませんでした。このことから、4-PBAはペルオキシソームを増加させることでミトコンドリアを伸長させていることが示唆されました。
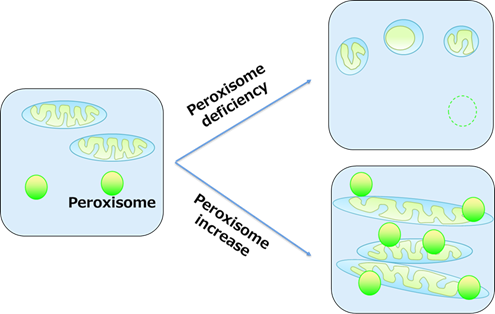
ここまでの結果から、ペルオキシソームの新たな機能としてミトコンドリアの動態を伸長方向へと制御していることが分かりました。次に私は、
②ペルオキシソームがミトコンドリアを制御する生物学的意義
について検証することにしました。
①: ペルオキシソームはどのようにミトコンドリア動態を制御しているのでしょうか?そこで注目したのは、ミトコンドリアの分裂を主に担う分子、Drp1です。この分子はミトコンドリアだけでなくペルオキシソームの分裂にも寄与していて、実際ペルオキシソームにもDrp1は局在することが知られています。そこで、
「ペルオキシソームはDrp1の制御を介してミトコンドリアの局在を調節する」という仮説を考え、検証することにしました。はじめにDrp1の局在を観察すると、ペルオキシソーム欠損細胞でミトコンドリア上のDrp1が増加していることが明らかになりました。さらに、このDrp1がペルオキシソーム欠損細胞におけるミトコンドリア断片化を起こしているのかを検証するためにDrp1のKDを行うと、ペルオキシソーム欠損細胞におけるミトコンドリア断片化は顕著に抑制されました。以上の結果より、ペルオキシソームはDrp1の局在制御を介してミトコンドリアの形態を制御することが分かりました。
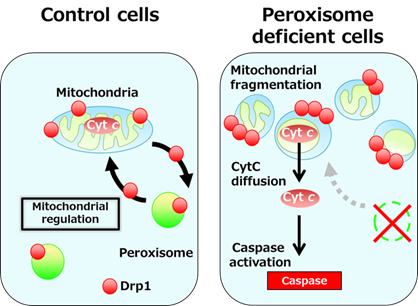
②ペルオキシソームがミトコンドリアの形態を制御する意義について、ペルオキシソームが欠損するとミトコンドリアが断片化することは先述しました。ミトコンドリアの断片化は膜間腔タンパク質シトクロムCの細胞質放出、並びにアポトーシス経路のカスパーゼ活性化にかかわります。そこでシトクロムCを観察すると、驚いたことにペルオキシソーム欠損細胞では通常ミトコンドリアにいるシトクロムC が細胞質に拡散していました。さらにこのとき、実行型カスパーゼの活性化も起こっていることも明らかになりました。すなわち、ペルオキシソームが欠損することで細胞死誘導経路が活性化していることが分かりました。では、その下流のアポトーシスは起こっているのでしょうか?
AnnexinV binding assayによって細胞のアポトーシスを検出すると、想定とは異なり、ペルオキシソーム欠損細胞ではアポトーシスはほとんど起きていませんでした。すなわち、ペルオキシソームの欠損によりシトクロムCの拡散・カスパーゼの活性化は起こるものの、アポトーシスを起こすには不十分であることが示唆されました。
では、この細胞死を起こさないsub-apoptoticなカスパーゼの活性化を抑制することにはどういった意味があるのでしょうか?私は、細胞のストレス感受性に注目しました。
我々の細胞は日々様々なストレス(酸化ストレス、小胞体ストレス、DNAダメージ、etc…)にさらされています。ストレスがかかった細胞は、まずそのストレスを解消するための経路を活性化させます。しかし、ストレスがかかり続けたり、過剰なストレスがかかったりした場合は、細胞はアポトーシスを選択します。私は、ペルオキシソームがミトコンドリアを介したストレスによるアポトーシスを調節している可能性を考えました。そのため、ペルオキシソーム欠損細胞にDNAダメージを添加し、アポトーシスを検出すると、通常細胞に比較してアポトーシスする細胞の割合が顕著に増加しました。このことから、ペルオキシソームによるカスパーゼ活性化調節は、細胞のストレス感受性にかかわることが示唆されました。
全体をまとめると、私は本論文においてペルオキシソームがDrp1の局在を介してミトコンドリアの動態を伸長方向へと制御している、という新たな機能を見出しました。この機能の破綻はミトコンドリアの断片化、シトクロムCの拡散、細胞死経路の活性化を引き起こすことも見出しました。
ミトコンドリアの形態は、様々な生命現象にかかわっています。先述のアポトーシスはもちろん、神経幹細胞の分化や、ニューロンの軸索におけるミトコンドリアの適切な配置にもミトコンドリア動態は重要です。本研究でミトコンドリア動態をペルオキシソームが制御することが明らかになったことにより、ペルオキシソームもまたそういった生命現象にかかわりうることが分かり、よりペルオキシソームの重要性が強調されたかと考えています。
さらに、本研究で見出したペルオキシソームによるミトコンドリアの形態制御の破綻が、先述のツェルベーガー症候群(ペルオキシソーム欠損症候群)の発症にかかわっている可能性もあります。特に、ミトコンドリア動態やカスパーゼの異常活性化は神経変性疾患にかかわるので、ツェルベーガー症候群における神経変性疾患様の症状にミトコンドリア動態制御破綻が関与する可能性を現在検証しています。
結果を丁寧に説明してきましたが、結局のところ私が読者の皆様に覚えておいていただきたいポイントは、「ペルオキシソームって結構大事なオルガネラなんだな」ということです。この機会にぜひ覚えておいてください!
発表論文
Peroxisomes control mitochondrial dynamics and the mitochondrion-dependent pathway of apoptosis, Journal of Cell Science, 2019
------
バイオステーションでは、筆頭著者の方による論文紹介を募集しています。どのような分量でも構いませんので、ぜひご寄稿いただけると幸いです。
詳細につきましては、以下のリンクもご覧ください
今後ともバイオステーションをよろしくお願いいたします。
神経前駆細胞の大移動@がん

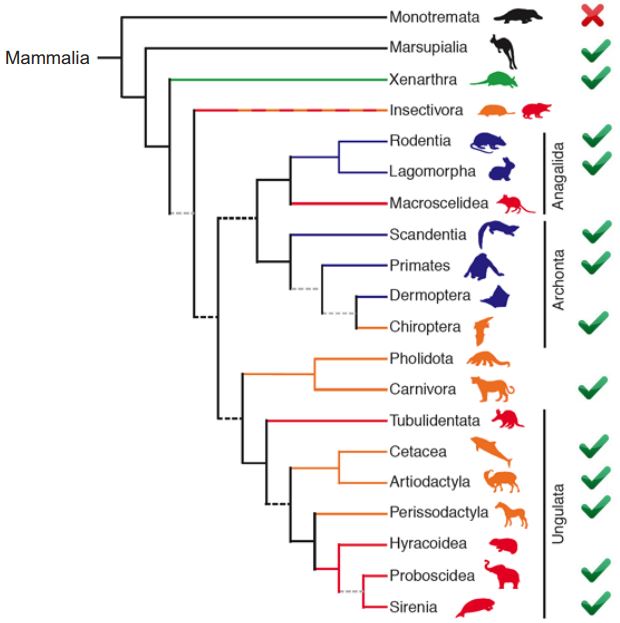
哺乳類の繁栄を支える遺伝子