ニューロンの多様性を作るメカニズム
私たちは常に外界からの情報を受け取り、処理し、行動に結びつけている。
ご存知のように、これらの情報処理を行うのに重要な器官は"脳"である。
人間には非常に多くのニューロンが存在するとされているが、
とても面白いことに、それぞれのニューロンはそれぞれ異なる特性を持ち、多様性があることが知られている。
多様なニューロンがぞれぞれのあるべき特性を獲得することは正常な脳機能に必須である。
-----
この中でこれまでに、ニューロンの多様性を生み出すのにプロトカドヘリン、という遺伝子が重要なことが報告されてきた。
プロトカドヘリンは細胞間接着で有名な因子、カドヘリンのスーパーファミリーに属し、細胞間の接着を制御する、細胞表面タンパク質である。
とてもとても興味深いことに、このプロトカドヘリンは多数のエクソンを持ち、その一つだけが1細胞(の1アレル)から選ばれて発現するということが知られている(Esumi et al., 2005など)。
下の図も参考に。
つまり、プロトカドヘリン(Pcdh-α)のV領域に存在する12個のエクソンα1~12のうち、一つだけが選ばれて発現する。
(ちゃんと言うならばプロトカドヘリンの一種、αとγがこのような制御を受ける。)
このように、プロトカドヘリンは1細胞ごとに発現するサブセットが異なる状態になる。
-----
この細胞ごとにプロトカドヘリンのサブセットが異なる性質は、脳発生にもとても重要であることが知られている。
一つ例をあげる。
この自己忌避の分子メカニズムは長い間不明であった。
ところが2012年、面白いことに、同じプロトカドヘリンのサブセットを発現している突起は互いに反発することが報告された。
この論文ではプロトカドヘリンの種類が一つになると(多様性がなくなると)自己忌避が抑制され、回路形成に異常がみられることを報告している。
すなわち、プロトカドヘリンサブセットがランダムに発現することがニューロンの多様性を生むのに重要である。
------
では、発現するプロトカドヘリンのエクソンはどのようにして選ばれるのだろうか??
------
(細かいが、プロトカドヘリンの発現量は低いのでcapture RNA seqというのを使っている。Cieslik, 2015)
すると、驚くべきことに、いくつかのプロトカドヘリンのエクソンからの転写がみられるとともに、プロトカドヘリンエクソンのアンチセンス(DNAの逆側、本来遺伝子をコードしない遺伝子)からRNAが発現していることが分かった。
これだけでも面白いがさらに、このノンコーディングRNAの転写がどこから開始されるのかを検証すると、このノンコーディングRNAは発現しているロトカドヘリンエクソンのセンス鎖RNAと同じプロモーターから転写が始まっていることが分かった。
*このように同じプロモーターから複数の転写物を出すようなプロモーターをconvergent promoterというらしい。珍しいし興味深い。
*これは、おそらく筆者らも想像していなかった結果だろう。とても驚き。
-----
- 単にプロトカドヘリンのエクソンが選ばれた結果発現しているものなのだろうか?
では、どのようにしてこの可能性を検証すればよいだろうか?
*CRIPSRa…CRISPR-cas9システムで用いるDNA切断酵素cas9のDNA切断活性をなくす。さらにcas9に転写を活性化させるタンパク質を結合させておく。これにより、ガイドRNAの配列依存的に転写を活性化させることができる。という系。
-----
詳細は省くが、彼らのモデルでは、
という流れをとるようだ。
さらに筆者らはin vivoにおいて、このスキームが重要であるかを検証した。
具体的にはDNAの脱メチル化を強制的に活性化させるため、DNA脱メチル化酵素Tet3の過剰発現マウスを作成し、解析した。
すると、Tet3を過剰発現すると、DNAの脱メチル化が亢進し、エンハンサーに最も近いプロモーターをもつプロトカドヘリンのエクソンが選択される傾向になることが分かった。
これは、Tet3の過剰発現によってランダムなプロトカドヘリンのエクソン選択がなくなってしまうことを意味する。
この結果によりDNAの脱メチル化がin vivoでも確かに重要であることが示唆された。
同様に、プロモーター-エンハンサーのループ形成で重要な役割をもつRad21を欠損させると、ループがなくなりプロトカドヘリンの発現も減少することを明らかにしている。
これらの結果から、ノンコーディングRNAの発現→DNAの脱メチル化→CTCFによるプロモーター-エンハンサーループの形成→コーディングRNAの発現、という流れがin vivoでも働いている可能性が示唆された。
-----
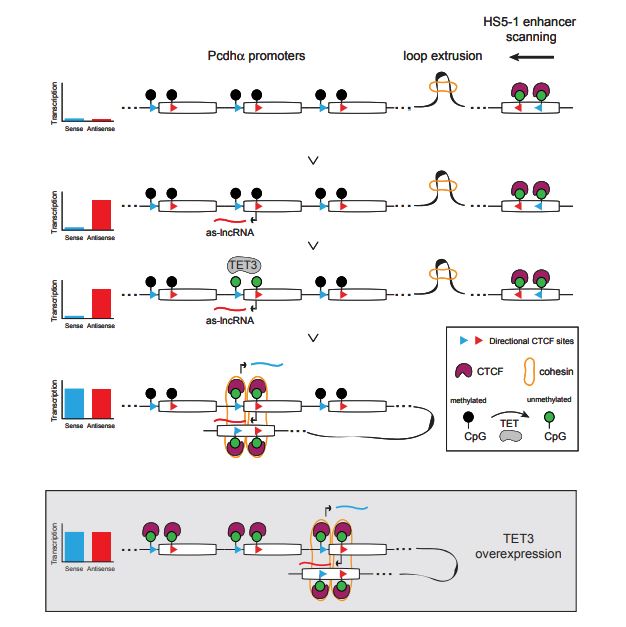
以下モデル図をお示しする(参考論文から引用)。
繰り返しにはなるが、
初めはセンス鎖からもアンチセンス鎖からも発現がない。
→DNAの脱メチル化(vivoでもtet3を介しているかは?)
→プロモーター-エンハンサーのループ形成
→選ばれたプロトカドヘリンエクソンの発現
という流れになる。
-----
素晴らしい研究ではあるが、気になる点もいくつかある。2つを紹介。
-----
さらに、最近シングルセル解析の発展により、ニューロンに限らず多様な細胞種でその多様性が報告されるようになっている。
一方、なぜ多様性が生まれるのか?という点についてはあまり研究が進んでいないように思われる。
これからの研究がとても楽しみ。
- 関連記事紹介
嗅覚受容体も細胞ごとに発現する遺伝子が異なることが知られている。
そのメカニズムに迫った論文を紹介しています。
-----
参考
- Antisense lncRNA Transcription Mediates DNA Demethylation to Drive Stochastic Protocadherin α Promoter Choice, Cell, 2019
- http://first.lifesciencedb.jp/archives/8634 (プロトカドヘリンの図の引用)